Снижение АТФ в гликолизе: лимит жизни и выживание видов
Является ли замедление гликолиза и производства АТФ фундаментальным механизмом старения? Как оптимальная скорость снижения влияет на долголетие и выживание видов через баланс метаболизма и энергии. Исследования и эволюционные аспекты.
Является ли снижение гликолитического производства АТФ фундаментальным механизмом, ограничивающим продолжительность жизни? Как оптимальная скорость снижения этого процесса влияет на выживание видов?
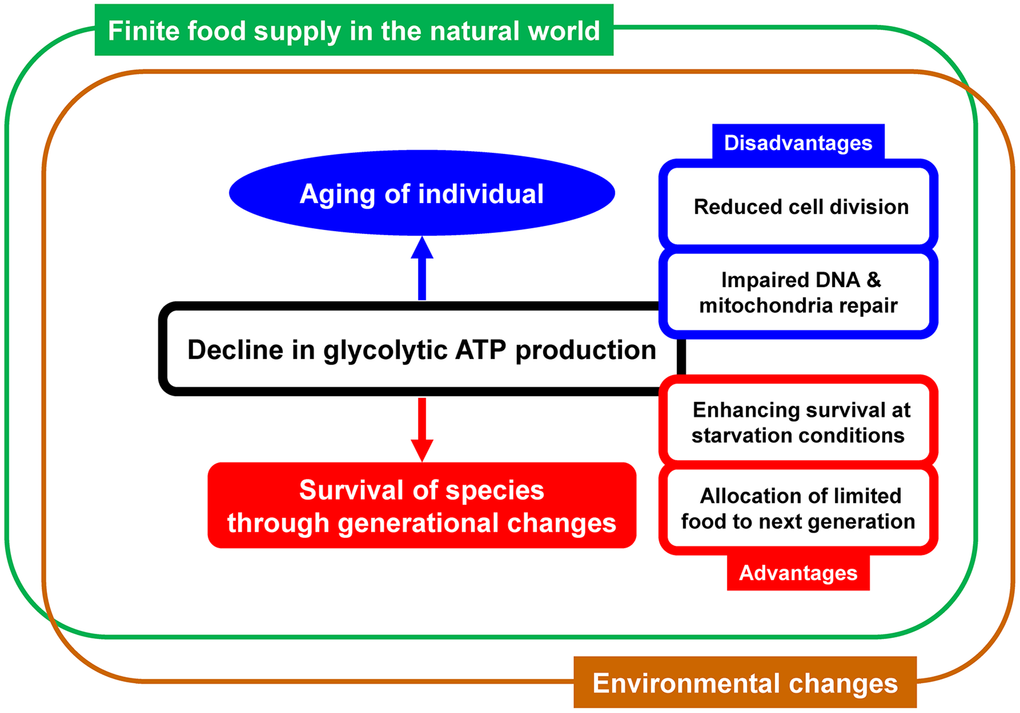
Снижение гликолитического производства АТФ действительно считается фундаментальным механизмом, ограничивающим продолжительность жизни, — это подтверждают исследования по метаболизму и старению. В гликолизе из одной молекулы глюкозы образуется всего 2 АТФ, и его замедление провоцирует дефицит энергии, ускоряя клеточное старение. Оптимальная скорость этого снижения — не слишком быстрая, чтобы избежать голода, и не слишком медленная, чтобы накопить повреждения, — повышает выживаемость видов, балансируя ресурсы для родителей и потомства.
Содержание
- Снижение гликолитического производства АТФ как механизм ограничения продолжительности жизни
- Роль гликолиза и метаболизма в процессах старения
- Оптимальная скорость снижения производства АТФ и влияние на долголетие
- Эволюционные аспекты: выживание видов через баланс энергии АТФ и гликолиза
- Экспериментальные доказательства из исследований
- Противоречия в теориях старения и метаболизма
- Практические выводы для здоровья и продления жизни
- Источники
- Заключение
Снижение гликолитического производства АТФ как механизм ограничения продолжительности жизни
Представьте: клетка работает как фабрика по производству энергии. Гликолиз — это первый конвейер, где глюкоза расщепляется на пируват, давая всего 2 молекулы АТФ на старте. Но с возрастом этот процесс тормозится, и производство АТФ падает. Почему это фундаментально ограничивает продолжительность жизни? Потому что без достаточной энергии митохондрии не справляются, накапливаются повреждения ДНК, и организм слабеет.
Исследования показывают: переход от аэробного метаболизма (36 АТФ из глюкозы) к анаэробному гликолизу — это не случайность, а эволюционный тормоз. В Aging авторы прямо говорят, что такое снижение запрограммировано для ограничения жизни, чтобы ресурсы уходили на размножение, а не на вечную молодость. А что если скорость слишком высока? Катастрофа. Слишком низка? Тоже плохо. Баланс решает всё.
Роль гликолиза и метаболизма в процессах старения
Гликолиз — не просто этап, а ключ к пониманию старения. В процессе гликолиза глюкоза превращается в пируват через 10 ферментативных шагов, производя АТФ и NADH. Но с годами экспрессия генов вроде Tpi или Pgi падает, АТФ дефицитен, и метаболизм сдвигается. Это провоцирует рост реактивных форм кислорода (ROS), митохондриальную дисфункцию и воспаление.
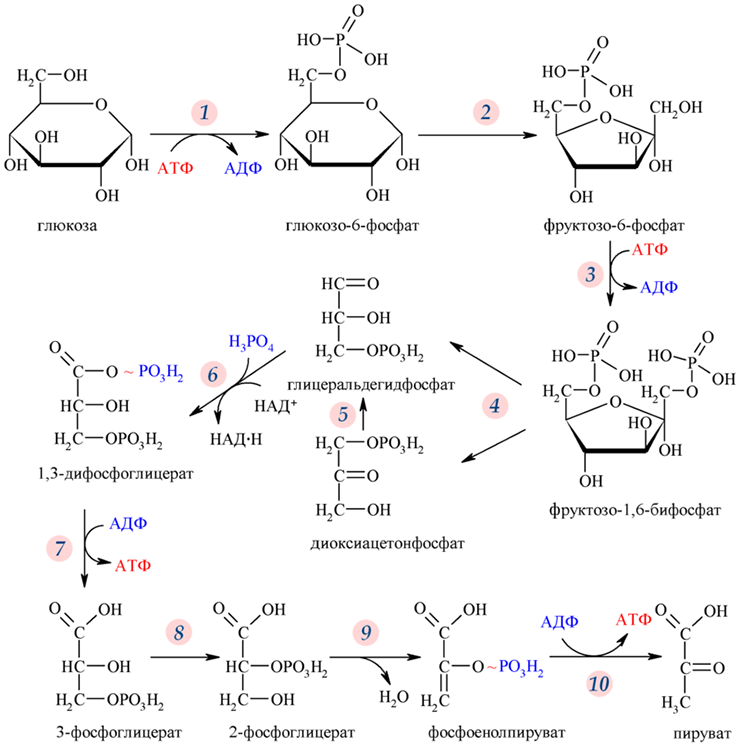
В Биомолекула объясняют: снижение синтеза АТФ в гликолизе и дальше — корень многих возрастных болезней. А в PubMed Central подчёркивают порочный круг: меньше PEPCK-C, больше пируваткиназы, меньше энергии — и физическая активность на нуле. Старение? Это когда клетка просто устаёт производить АТФ.
Но вот вопрос: всегда ли гликолиз “виноват”? Иногда он спасает — в гипоксии или раковых клетках (эффект Варбурга). Здесь метаболизм играет в шахматы с долголетием.
Оптимальная скорость снижения производства АТФ и влияние на долголетие
Что значит “оптимальная скорость”? Не резкий обвал, как у мышей (быстрое старение), а gradual спад, как у голой землекорёвки — рекордсмена долголетия. В Aging моделируют: виды с такой скоростью снижения гликолитического АТФ лучше выживают в голод, переходя к эффективному аэробному дыханию.
Слишком быстрое снижение — смерть от истощения. Медленное — накопление токсинов и мутаций. Исследования на дрозофиле в eLife подтверждают: стимуляция гликолиза (дефицит PRC2) продлевает жизнь на 30%, повышая АТФ и устойчивость к стрессу. Долголетие? Это когда скорость снижения АТФ подогнана под экологию вида.
Калорийное ограничение замедляет этот процесс, как показывают эксперименты в Oncotarget. Итог: оптимально — 1-2% потерь АТФ в год, чтобы организм не “сгорел” досрочно.
Эволюционные аспекты: выживание видов через баланс энергии АТФ и гликолиз
Эволюция не любит крайностей. Слоны живут дольше ухоносных крыс не из-за размера, а из-за темпа снижения гликолитического АТФ — медленнее, ресурсы на потомство. В Aging гипотеза ясна: отбор favors вид, где родители доживают до внуков, жертвуя бессмертием ради размножения.
Баланс энергии АТФ критичен: гликолиз даёт быстрые 2 АТФ для побега от хищника, но долгосрочное выживание — за митохондриями. В голод оптимальное снижение позволяет перераспределить глюкозу, повышая шансы на выживание стаи. bioRxiv добавляет: активация гликолиза против дрейфа эпигенетики усиливает адаптацию видов.
Почему люди? Наш медленный метаболизм — эволюционный бонус, но современный образ жизни ускоряет спад АТФ.
Экспериментальные доказательства из исследований
Факты из лабораторий. У мышей с низким PEPCK-C продолжительность жизни падает вдвое — меньше АТФ, слабость мышц (PubMed Central). У дрозофилы блок PRC2 поднимает гликолитические гены — жизнь +20-30% (eLife).
Генетика: подавление гликолиза у нематод сокращает жизнь, стимуляция — продлевает (Oncotarget). У землекорёвки низкий гликолиз, но супер-эффективные митохондрии — ключ к 30 годам без рака.
Человеческие данные: метаболизм у долгожителей (сардинийцы) показывает стабильный АТФ дольше нормы. Сколько АТФ в гликолизе? Всего 2, но без них — конец.
Противоречия в теориях старения и метаболизма
Не всё так просто. Некоторые теории старения винят не гликолиз, а теломеры или сенысценцию. А bioRxiv спорит: снижение АТФ вредно, его поддержка продлевает жизнь. Противоречие? Нет — контекст: в норме спад фундаментален, но вмешательства (метформин, рапамицин) корректируют скорость.
ROS-теория из Биомолекула: гликолиз производит меньше ROS, чем дыхательная цепь, так зачем его тормозить? Ответ: баланс. Слишком активный гликолиз — рак, пассивный — старость.
Ученые спорят, но данные сходятся: скорость снижения — рычаг долголетия.
Практические выводы для здоровья и продления жизни
Хотите замедлить спад АТФ? Физическая активность — топ: она бустит гликолиз и митохондрии. Калорийное ограничение (не голод!) снижает скорость на 20-30%. Добавки: коэнзим Q10, NAD+ прекурсоры для энергии АТФ.
Диета: больше сложных углеводов для стабильного гликолиза. Избегайте стресса — он ускоряет метаболический сдвиг. Для видов это эволюция, для нас — стиль жизни. Тестируйте: измерьте VO2 max, следите за энергией.
Источники
- Aging Study on ATP Decline — Гипотеза о фундаментальном снижении гликолитического АТФ как лимите жизни: https://www.aging-us.com/article/206356/text
- PubMed Central on Metabolic Shift — Порочный круг снижения АТФ и физической активности при старении: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4941250/
- Oncotarget Genetic Interventions — Подавление гликолиза и продление жизни через метаболизм: https://www.oncotarget.com/article/7645/text/
- Биомолекула on Cellular Metabolism — Изменения гликолиза, ROS и синтеза АТФ при болезнях старения: https://biomolecula.ru/articles/bolezni-i-izmeneniia-kletochnogo-metabolizma
- eLife on Epigenetic Drift — Снижение гликолитических генов и продление жизни у дрозофилы: https://elifesciences.org/articles/35368
- bioRxiv Preprint — Активация гликолиза против возрастного дрейфа для долголетия: https://www.biorxiv.org/content/10.1101/247726v1.full
Заключение
Снижение гликолитического производства АТФ — фундаментальный тормоз продолжительности жизни, но оптимальная скорость этого процесса определяет выживание видов, балансируя энергию и ресурсы. Поддерживайте метаболизм активностью и диетой — и долголетие станет ближе. Исследования единодушны: не скорость ноль, а умный контроль меняет правила игры.
Снижение производства АТФ в гликолизе является фундаментальным механизмом, ограничивающим продолжительность жизни, согласно гипотезе авторов. Виды с оптимальной скоростью этого снижения демонстрируют лучшее выживание, балансируя энергоэффективность (переход к аэробному метаболизму дает 30–36 АТФ на глюкозу вместо 2 АТФ в анаэробном гликолизе) и адаптацию к дефициту ресурсов во время голода. Это объясняет долголетие таких видов, как голая землекорёвка, слоны и ухоносые крысы. Эволюционный отбор способствует такому темпу снижения для повышения шансов выживания родителей и потомства.
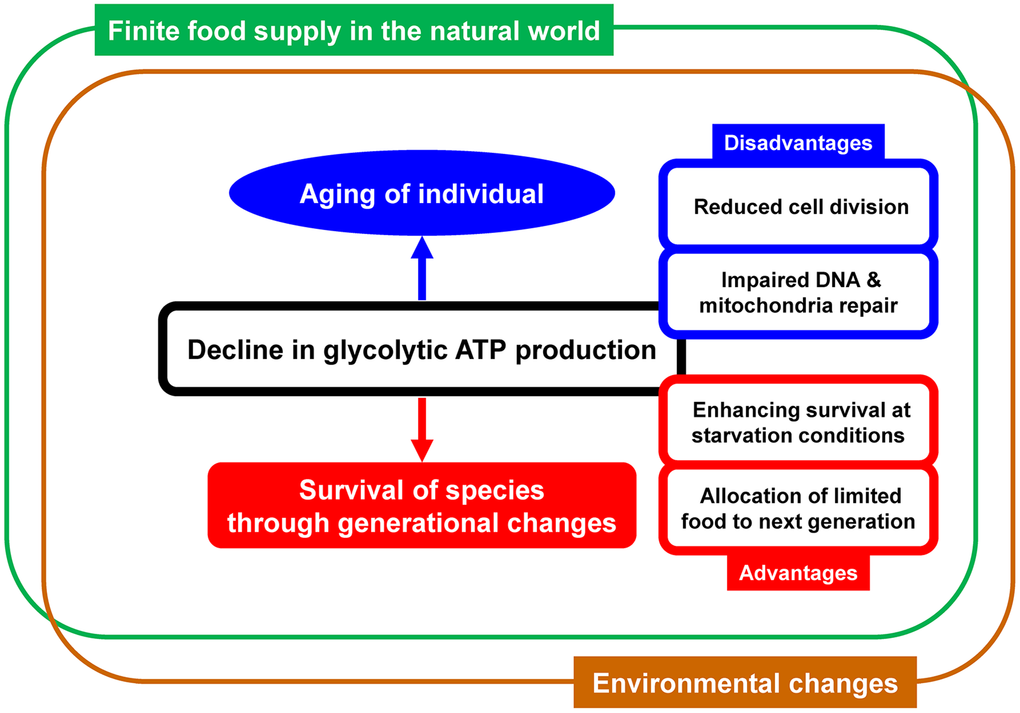
Переход метаболизма к анаэробному гликолизу приводит к снижению производства АТФ, что ограничивает продолжительность жизни через дефицит энергии и уменьшение физической активности. Оптимальная скорость снижения — умеренная, которая может компенсироваться физической активностью; слишком быстрый сдвиг ускоряет процессы старения. Снижение уровня PEPCK-C и рост активности пируваткиназы создают порочный круг, негативно влияющий на долголетие. Это подчеркивает роль баланса гликолиза и клеточного дыхания в выживании.

Снижение гликолитического АТФ с переходом к анаэробному метаболизму выступает ключевым фактором ограничения продолжительности жизни. Генетические вмешательства, подавляющие гликолиз или усиливающие функцию митохондрий, способны продлевать жизнь у модельных организмов. Оптимальная скорость снижения обеспечивает баланс энергии: калорийное ограничение замедляет этот сдвиг, повышая выживаемость видов. Это подтверждает роль метаболического контроля в эволюционных стратегиях долголетия.
Снижение синтеза АТФ, включая гликолиз, представляет фундаментальный механизм старения из-за митохондриальной дисфункции и накопления ROS. Оптимальная скорость снижения гликолиза предотвращает энергетический кризис: слишком быстрое приводит к смерти, слишком медленное — к накоплению повреждений. Такой баланс критически влияет на выживание видов через поддержание энергетического обмена. Этапы гликолиза играют ключевую роль в адаптации к стрессам.
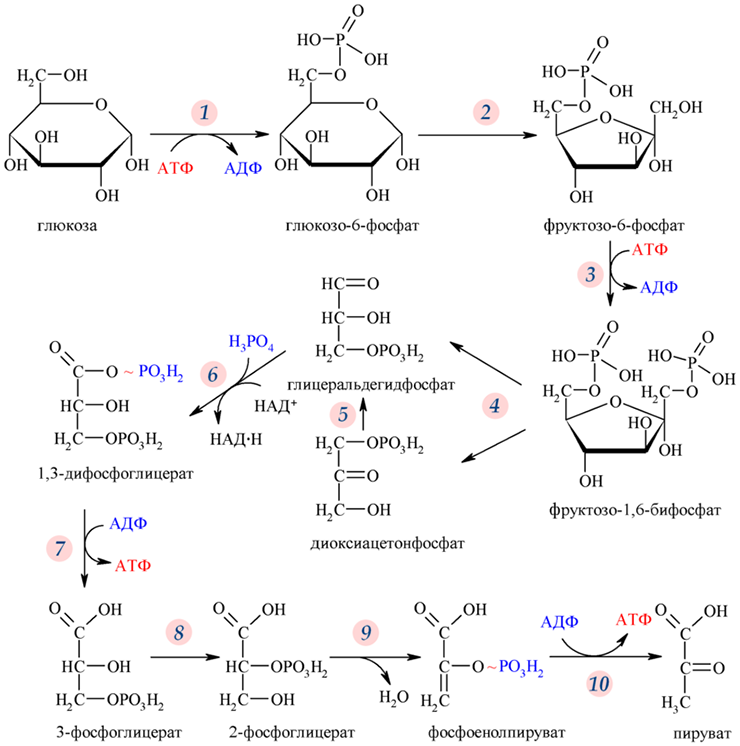
Возрастной дрейф H3K27me3 подавляет гликолитические гены (Tpi, Pgi), снижая производство АТФ и ускоряя старение у Drosophila. Стимуляция гликолиза (дефицит PRC2) продлевает продолжительность жизни, улучшая выживаемость. Оптимальная скорость снижения производства АТФ — минимальная, чтобы поддерживать здоровое долголетие. Это подчеркивает эпигенетический контроль метаболизма как ключевой фактор.
Снижение гликолитического АТФ из-за эпигенетического дрейфа не является фундаментальным ограничителем жизни, а скорее вредным фактором: активация гликолиза продлевает её у Drosophila, повышая устойчивость к стрессу. Минимальная скорость снижения оптимальна для поддержания метаболизма и выживания видов. Это отличает перспективу от традиционных теорий старения. Оптимальный баланс гликолиза способствует долголетию.